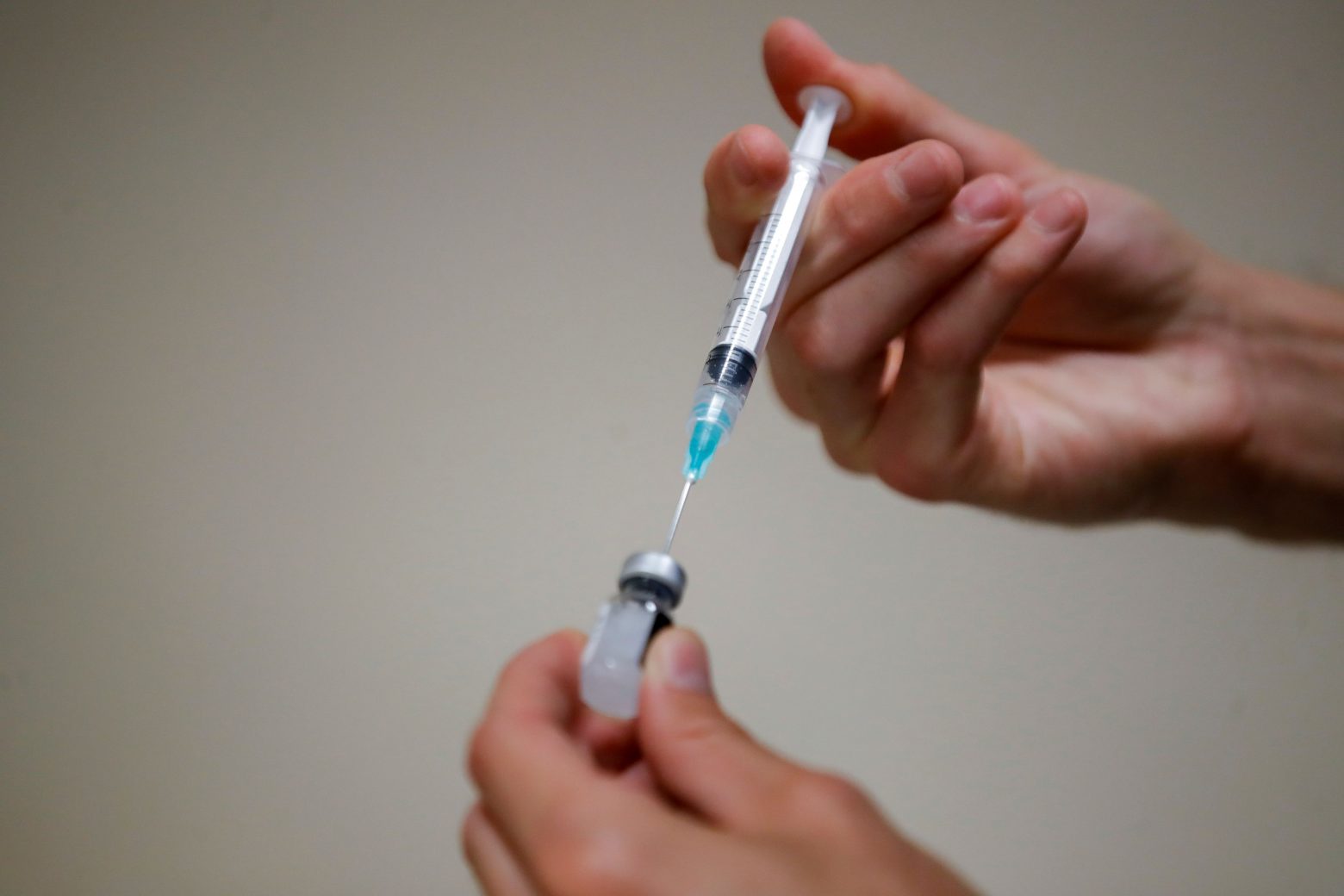
Κοροναϊός: Οι φαρμακοβιομηχανίες καλούνται να επεκτείνουν τις μελέτες ασφαλείας για τον εμβολιασμό παιδιών
Τέλη του έτους αναμένονται τα παιδιατρικά εμβόλια της Pfizer και της Moderna
Spotlight
-

Μένει χωρίς ερευνητικό σκάφος η Ελλάδα – Το ωκεανογραφικό «Αιγαίο» αποσύρεται
-

Αυξημένα μέτρα της Τροχαίας για την περίοδο εορτασμού του Πάσχα και της Πρωτομαγιάς
-

Η Ισπανία επιβεβαιώνει την αποστολή πυραύλων Patriot στην Ουκρανία
-

5.000 δολάρια το κεφάλι – Οι κερδοσκόποι του πολέμου και το τίμημα της σωτηρίας από την κόλαση της Γάζας
Με αίτημα των αμερικανικών ομοσπονδιακών αρχών, οι εταιρείες Pfizer και Moderna επεκτείνουν το δείγμα των κλινικών μελετών για τη χρήση των εμβολίων Covid-19 σε παιδιά 5 -11 ετών, ένα προληπτικό μέτρο για την καταγραφή τυχόν σπάνιων παρενεργειών όπως η φλεγμονή της καρδιάς που αναφέρθηκε σε λίγους εμβολιασμένους κάτω των 30 ετών.
Σε τοπική πολιτική συγκέντρωση στο Οχάιο την περασμένη εβδομάδα, ο πρόεδρος Τζο Μπάιντεν δήλωσε ότι η έκτακτη αδειοδότηση των παιδιατρικών εμβολίων θα έρθει «σύντομα» χωρίς όμως να διευκρινίσει πότε.
Πηγές των New York Times που γνωρίζουν το θέμα ανέφεραν ότι η Υπηρεσία Τροφίμων και Φαρμάκων (FDA) ενημέρωσε τη Pfizer και τη Moderna ότι ο αριθμός των παιδιών που σχεδίαζαν να εντάξουν στις δοκιμές ήταν ανεπαρκής για την ανίχνευση πολύ σπάνιων παρενεργειών –όσο μεγαλύτερο είναι το στατιστικό δείγμα της μελέτης, τόσο πιο σπάνιες ανεπιθύμητες δράσεις μπορούν να γίνουν αντιληπτές.
Οι ρυθμιστικές αρχές θα πρέπει να ζυγίζουν τα οφέλη του εμβολίου έναντι των κινδύνων της Covid-19, οι οποίοι θεωρούνται μικρότεροι για τα παιδιά.
Οι αμερικανικές και οι ευρωπαϊκές αρχές έχουν πάντως διαβεβαιώσει ότι τα οφέλη υπερσταθμίζουν ξεκάθαρα το ρίσκο για τις ηλικίες 12 ετών και άνω. Για τη συγκεκριμένη ηλικιακή ομάδα έχει εγκριθεί εδώ και μήνες στις ΗΠΑ το εμβόλιο της Pfizer, ενώ στην Ευρώπη έχουν λάβει άδεια τα εμβόλια της Pfizer και πιο πρόσφατα της Moderna.
Σύμφωνα με τα αμερικανικά Κέντρα Ελέγχου και Πρόληψης Νοσημάτων (CDC), ο κίνδυνος μυοκαρδίτιδας ή περικαρδίτιδας σε νεαρούς λήπτες των εμβολίων mRNA είναι πολύ μικρός, με λιγότερα από 13 περιστατικά ανά εκατομμύριο δόσεις.
Στη μεγάλη πλειονότητα των περιπτώσεων, η φλεμονή της καρδιάς είναι ήπια και υποχωρεί σε διάστημα μερικών ημερών.
Η FDA ζήτησε από τις δύο εταιρείες να εντάξουν στις μελέτες τουλάχιστον 3.000 παιδιά 5-11 ετών. Ο αριθμός είναι διπλάσιος από αυτόν που προγραμμάτιζε η Pfizer. Η εταιρεία σκόπευε να εντάξει 4.500 παιδιά κάτω των 12, χωρισμένες σε μια ομάδα 5-11 ετών και δύο ισάριθμες ομάδες μικρότερων ηλικιών.
Εκπρόσωπος της Moderna επβεβαίωσε στους NY Times ότι η εταιρεία δέχτηκε να χρησιμοποιήσει μεγαλύτερο αριθμό εθελοντών, «κάτι που αυξάνει την πιθανότητα ανίχνευσης σπάνιων συμβάντων».
Η Moderna εκτιμά ότι θα υποβάλλει αίτημα επείγουσας αδειοδότησης στα τέλη του 2021 με αρχές του 2022, ενώ η Pfizer εκτιμάται ότι προηγείται.
Ακολουθήστε το in.gr στο Google News και μάθετε πρώτοι όλες τις ειδήσεις

















































 Αριθμός Πιστοποίησης Μ.Η.Τ.232442
Αριθμός Πιστοποίησης Μ.Η.Τ.232442