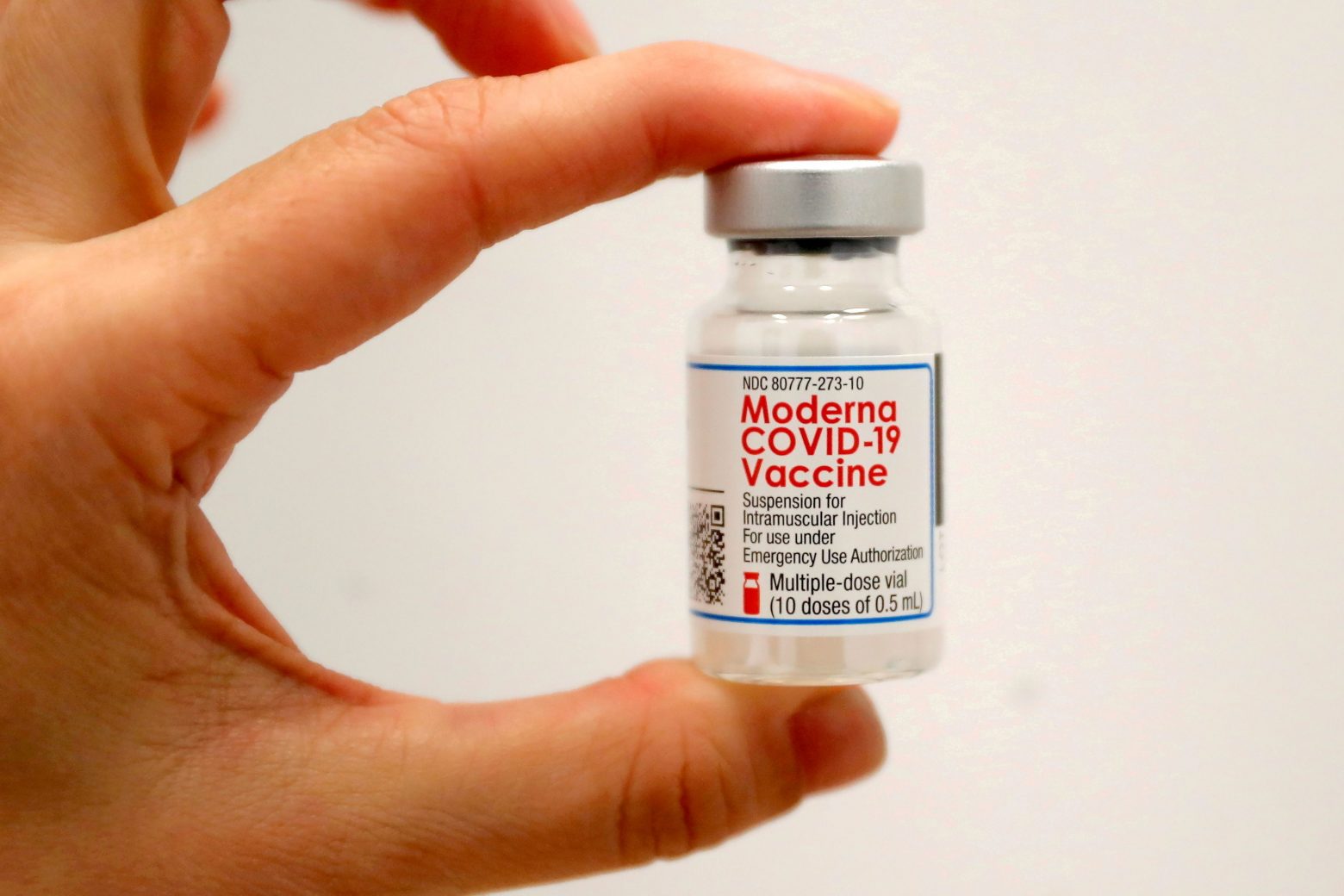
Moderna – Προ των πυλών η πλήρης έγκριση του εμβολίου στις ΗΠΑ
Με την κατάθεση των συμπληρωματικών επιστημονικών στοιχείων από την εταιρεία στις αρμόδιες υγειονομικές αρχές, η διαδικασία αναμένεται να είναι γρήγορη, καθώς ιδανικά η πλήρης έγκριση θα πρέπει να έχει διασφαλιστεί πριν τις 20 Σεπτεμβρίου.
Spotlight
-

Συγκρούσεις στη Μέση Ανατολή, πόλεμος στην Ουκρανία, πυρηνικές απειλές – Οδεύουμε στον Τρίτο Παγκόσμιο Πόλεμο;
-

Αυτό που θα δεις πρώτα στην εικόνα αποκαλύπτει πολλά για την προσωπικότητά σου
-

ΚΕΠΕ: Ανησυχητικά τα στοιχεία για την παιδική φτώχεια – Να είμαστε σε διαρκή εγρήγορση
-

Ο άνθρωπος-κόλεϊ από την Ιαπωνία ξαναχτυπά με νέα βίντεο εναντίον Ακίτα
Αίτηση για να λάβει πλήρη έγκριση για το εμβόλιο της κατέθεσε και η Moderna, η οποία παρέδωσε στις αρμόδιες αμερικανικές αρχές όλα τα απαιτούμενα συμπληρωματικά στοιχεία κλινικών μελετών και επιστημονικών στοιχείων αναφορικά με την δράση του σκευάσματος της.
Σύμφωνα με ανακοίνωση της, μέχρι πριν δύο χρόνια, άγνωστης εταιρεία βιοτεχνολογίας, η Moderna ζήτησε πλήρη έγκριση για τη χορήγηση του mRNA σκευάσματος της, που χορηγείται σε δύο δόσεις, σε όσους είναι άνω των 18 ετών. Κίνηση που έρχεται μόλις δύο ημέρες, αφότου η υπηρεσία του Food and Drug Administration (FDA) έδωσε την πολυπόθητη πλήρη έγκριση στο αντίστοιχο εμβόλιο των Pfizer/BioNTech.
Κατά την ανακοίνωση της, η εταιρεία δήλωσε επίσης πως οι τελικές κλινικές μελέτες που υποβλήθηκαν προς τις αρχές δείχνουν πως η αποτελεσματικότητα του εμβολίου της Moderna παραμένει πολύ ψηλά, στο 93%, μέχρι και έξι μήνες μετά τη χορήγηση και της δεύτερης δόσης.
Τόσο η Moderna όσο και η Pfizer είχαν λάβει έγκριση έκτακτης ανάγκης για τη χορήγηση του εμβολίου τους, τον περασμένο Δεκέμβριο, κάτι που επέτρεψε την συμμετοχή τους στο εθνικό εμβολιαστικό πρόγραμμα των ΗΠΑ, αλλά άφηνε νομικά κενά.
Με την άδεια πλήρους έγκρισης, τα εμβόλια παραμένουν μόνιμα διαθέσιμα στην αγορά, ενώ νομικά γίνεται ευκολότερο για φορείς και εταιρείες να καταστήσουν υποχρεωτικό τον εμβολιασμό των εργαζομένων με τα συγκεκριμένα σκευάσματα.
Σύμφωνα με αναλυτές, η διασφάλιση πλήρους έγκρισης και από την Moderna θα προχωρήσει γρήγορα και αυτό διότι οι αρχές θέλουν να διευκολύνουν τις επιχειρήσεις να αυξήσουν την πίεση για τον εμβολιασμό των εργαζομένων πριν το χειμώνα, ενώ είναι απαραίτητη και για το πρόγραμμα των ενισχυτικών δόσεων που έχει αναγγελθεί πως θα ξεκινήσει από τα τέλη Σεπτεμβρίου. Το τελευταίο σημαίνει πως ιδανικά η πλήρης έγκριση θα πρέπει να έχει διασφαλιστεί πριν τις 20 Σεπτεμβρίου.
Ακολουθήστε το in.gr στο Google News και μάθετε πρώτοι όλες τις ειδήσεις














































 Αριθμός Πιστοποίησης Μ.Η.Τ.232442
Αριθμός Πιστοποίησης Μ.Η.Τ.232442